Pengertian Benzena
Benzena merupakan suatu produk minyak bumi yang awalnya terbuat dari batubara yang dipakai sebagai komponen dalam berbagai produk konsumen dan industri. Benzena ini ditemukan oleh Faradat kemudian rumus molekulnya ditetapkan oleh Mitscherlich sebagai C6H6. Benzena ini termasuk dalam golongan senyawa hidrokarbon. Benzena mempunyai derajat kejenuhan yang tinggi.
Senyawa benzena dan sejumlah turunannya digolongkan dalam senyawa aromatik, yang mana penggolongan ini dilandasi oleh aroma yang dipunyai sebagian dari senyawa-senyawa tersebut. Akan tetapi para kimiawan sekarang tidak lagi mengklasifikasikan senyawa kimia yang berdasarkan sifat fisiknya lagi, melainkan berdasarkan struktur dan kereaktifannya.
Sifat-Sifat Benzena
Pada umumnya, sifat senyawa bisa dikelompokkan menjadi dua, yakni sifat fisik dan sifat kimia.
1. Sifat Fisik
Benzena adalah suatu zat cair tidak berwarna, mudah menguap, dan sangat beracun. Benzena bisa diapaki sebagai pelarut, pensintesis berbagai senyawa karbon, dan bahan dasar pembuatan senyawa karbon. Benzena tidak begitu reaktif, tapi sangat mudah terbakar, karena kadar karbon yang terkandung sangat tinggi.
Benzena adalah suatu zat cair tidak berwarna, mudah menguap, dan sangat beracun. Benzena bisa diapaki sebagai pelarut, pensintesis berbagai senyawa karbon, dan bahan dasar pembuatan senyawa karbon. Benzena tidak begitu reaktif, tapi sangat mudah terbakar, karena kadar karbon yang terkandung sangat tinggi.
Beberapa turunan dari benzena ada yang bersifat polar maupun non polar. Senyawa polar yaitu suatu senyawa yang terbentuk akibat adanya suatu ikatan antar elektron pada unsur-unsurnya. Titik didih pada benzena dan turunannya dimulai dari 80-250 derjat celsius. Untuk titik lelehnya bervariasi, dengan angka tertinggi yaitu 122 derjat celsius pada senyawa asam benzoat (-COOH).
Variasi titik didih tersebut dikarenakan oleh perngaruh dari kepolaran gugus fungsionalnya. Begitu juga dengan titik lelehnya, dipengaruhi oleh subtitutenya. Seperti benzena, toluena, dan etil benzena bersifat non-polar. Sedangkan anilin, benzil alkoho, fenol, dan asam benzoat bersifat polar. Maka bisa disimpulkan asam benzoat mempunyai titik didih tertinggi, dikarenakan sifat polarnya yang lebih, sedangkan benzena memiliki titik didih terendah.
Senyawa turunan benzena yang sifatnya non-polar tidak akan larut dalam air, sebaliknya, yang bersifat polar akan larut didalam air.
2. Sifat Kimia
Derajat keasaman adalah salah satu sifat kimia benzena dan turunannya. Fenol dan asam benzoat termasuk asam lemah. Asam benzoat lebih kuat dibandingkan fenol. Fenol yang mempunyai gugus fungsi -OH ternyata bersifat asam lemah, yang berarti memberikan ion H+, sedangkan anilin yang memiliki gugus –NH2 bersifat basa lemah, yang berarti menerima ion H+.
Benzena lebih mudah mengalami reaksi subtitusi daripada reaksi adisi.
Derajat keasaman adalah salah satu sifat kimia benzena dan turunannya. Fenol dan asam benzoat termasuk asam lemah. Asam benzoat lebih kuat dibandingkan fenol. Fenol yang mempunyai gugus fungsi -OH ternyata bersifat asam lemah, yang berarti memberikan ion H+, sedangkan anilin yang memiliki gugus –NH2 bersifat basa lemah, yang berarti menerima ion H+.
Benzena lebih mudah mengalami reaksi subtitusi daripada reaksi adisi.
Reaksi Benzena
Reaksi yang umum terjadi yaitu suatu reaksi subtitusi elektrofilik, ada 4 macam, yakni sebagai berikut :
1. Subtitusi dengan halogen (Halogenasi)
Benzena mengalami subtitusi dengan halogen memakai katalisator besi (III) halida.
Benzena mengalami subtitusi dengan halogen memakai katalisator besi (III) halida.
Contohnya:
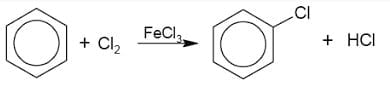
2. Subtitusi dengan asam nitrat (Nitrasi)
Benzena bereaksi dengan asam nitrat pekat memakai katalisator asam sulfat pekat membentuk nitrobenzena.
Benzena bereaksi dengan asam nitrat pekat memakai katalisator asam sulfat pekat membentuk nitrobenzena.
Contohnya:
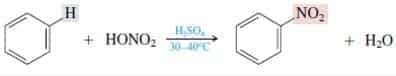
3. Subtitusi dengan asam sulfat pekat (Sulfonasi)
Sulfonasi terjadi Bila benzena dipanaskan dengan asam sulfat pekat.
Sulfonasi terjadi Bila benzena dipanaskan dengan asam sulfat pekat.
Contoh:
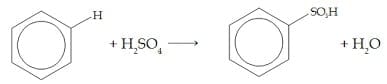
4. Subtitusi dengan alkil halida (Alkilasi)
Reaksi ini bisa memakai untuk membentuk alkil benzena menggunakan katalisator alumunium klorida (AlCl3).
Reaksi ini bisa memakai untuk membentuk alkil benzena menggunakan katalisator alumunium klorida (AlCl3).
Contohnya:
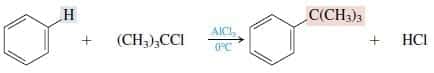
Tatanama Benzena
1. Benzena Monosubtitusi
Benzena dengan satu subtituen alkil diberi nama sebagai turunan benzena, misalnya etilbenzena. Sistem IUPAC tetap memakai nama umum untuk beberapa benzena monosubstitusi, misalnya toluena, kumena, stirena.
Benzena dengan satu subtituen alkil diberi nama sebagai turunan benzena, misalnya etilbenzena. Sistem IUPAC tetap memakai nama umum untuk beberapa benzena monosubstitusi, misalnya toluena, kumena, stirena.
Nama-nama umum seperti fenol, anilina, benzaldehida, asam benzoat, anisol juga tetap dipakai dalam sistem IUPAC. Sistem IUPAC (International Union Pure and Applied Chemistry) yaitu suatu lembaga yang berwewenang untuk merumuskan tata nama senyawa.
2. Benzena Disubtitusi
Disubtitusi berarti benzena mengikat dua subtituen, maka terdapat kemungkinan mempunyai tiga isomer struktur. bila kedua subtituen diikat oleh atom-atom karbon 1,2- disebut orto (o) satu sama lain, jika karbon 1,3- disebut meta (m), dan 1,4 disebut para (p).
Disubtitusi berarti benzena mengikat dua subtituen, maka terdapat kemungkinan mempunyai tiga isomer struktur. bila kedua subtituen diikat oleh atom-atom karbon 1,2- disebut orto (o) satu sama lain, jika karbon 1,3- disebut meta (m), dan 1,4 disebut para (p).
Sistem IUPAC memakai nama umum xilena untuk ketiga isomer dimetilbenzena, yakni o-xilena, m-xilena, dan p-xilena. jika kedua substituen tersebut tidak memberikan nama khusus, maka masing-masing dari substituen diberi nomor, dan namanya akan diurutkan berdasarkan urutan abjad, dan diakhiri dengan kata benzena. Atom karbon yang mengikat substituen yang urutan abjadnya lebih dahulu diberi nomor 1.
3. Benzena Polisubtitusi
Benzena polisubtitusi yaitu ketika terdapat tiga atau lebih substituen terikat pada cincin benzena, maka posisi masing-masing substituen ditunjukkan dengan nomor. Bila salah satu substituen memberikan nama khusus, maka diberi nama senyawanya sebagai turunan dari nama khusus tersebut. Dan bila semua substituen tidak memberikan nama khusus, maka posisisnya akan dinyatakan dengan nomor dan diurutkan sesuai urutan abjad, dan diakhiri dengan kata benzena.
Benzena polisubtitusi yaitu ketika terdapat tiga atau lebih substituen terikat pada cincin benzena, maka posisi masing-masing substituen ditunjukkan dengan nomor. Bila salah satu substituen memberikan nama khusus, maka diberi nama senyawanya sebagai turunan dari nama khusus tersebut. Dan bila semua substituen tidak memberikan nama khusus, maka posisisnya akan dinyatakan dengan nomor dan diurutkan sesuai urutan abjad, dan diakhiri dengan kata benzena.
Rumus Struktur Benzena
Struktur benzena dituliskan sebagai cincin beranggota enam (heksagonal) yang mengandung ikatan tunggal dan rangkap berselang-seling.
Struktur kekue, menggambarkan penggantian sembarang atom brom pada hidrogen akan menghasilkan senyawa sama, karena keenam atom karbon dan hidrogen ekivalen. Kekule ini bisa menjelaskan fakta bahwa bila benzena bereaksi dengan brom memakai katalis FeCl3 hanya menghasilkan satu senyawa yang mempunyai rumus molekul C6H5Br.
Cincin benzena disajikan dalam bentuk segienam beraturan dengan sebuah lingkaran didalamnya, dengan ketentuan bahwa pada setiap sudut segienam tersebut terikat sebuah atom H.
Klasifikasi Dan Penggunaan Benzena
Berikut ini ialah beberapa turunan benzena serta penggunaanya dalam kehidupan sehari-hari yaitu sebagai berikut :
1. Benzena
Benzena banyak dipakai sebagai pelarut, bahan dasar pembuatan monomer stirena (C6H6 – CH = CH2). Monomer stirena adalah bahan polimer untuk membuat karet sintetis, bahan pestisida, pemanis buatan. Selain itu benzena juga dipakai sebagai bahan dasar nilon.
Benzena banyak dipakai sebagai pelarut, bahan dasar pembuatan monomer stirena (C6H6 – CH = CH2). Monomer stirena adalah bahan polimer untuk membuat karet sintetis, bahan pestisida, pemanis buatan. Selain itu benzena juga dipakai sebagai bahan dasar nilon.
2. Asam Benzoat (C6H5COOH)
Asam benzoat atau garam natriumnya dipakai sebagai pengawet berbagai makanan atau olahan minuman. Asam atau garam ini dipilih karena tidak mempengaruhi cita rasa makanan yang diawetkan.
Asam benzoat atau garam natriumnya dipakai sebagai pengawet berbagai makanan atau olahan minuman. Asam atau garam ini dipilih karena tidak mempengaruhi cita rasa makanan yang diawetkan.
3.Fenol (C6H5OH)
Fenol bisa mematikan mikroorganisme sehingga dipakai untuk pembasmi kuman seperti pembersih lantai (karbol).
Fenol bisa mematikan mikroorganisme sehingga dipakai untuk pembasmi kuman seperti pembersih lantai (karbol).
4. Asam Salisilat
Asam ini dikenal dengan asam o-hidroksibenzoat. Ini banyak dipakai sebagai bahan antiseptik pada kulit seperti bedak kulit. Juga sebagai pemghilang rasa sakit kepala seperti aspirin.
Asam ini dikenal dengan asam o-hidroksibenzoat. Ini banyak dipakai sebagai bahan antiseptik pada kulit seperti bedak kulit. Juga sebagai pemghilang rasa sakit kepala seperti aspirin.
Itulah ulasan tentang Benzena : Pengertian, Sifat, Reaksi, Tatanama, Klasifikasi, Dan Rumus Struktur Beserta Contoh Lengkap Semoga apa yang diulas diatas bermanfaat bagi pembaca. Sekian dan terimakasih.













Don't Miss Any Update, Join Us on Social Networks.